Imprimez gratuitement des calendriers, agendas et emplois du temps (année scolaire 2024-2025) !
Editions Petite Elisabeth. Des ressources pédagogiques en mathématiques, physique et chimie pour les collèges, les lycées et la formation professionnelle (CAP, BEP, BP et bac pro).
Électrolyse de l'eau
Calculer le volume de dioxygène O2 formé à l'anode et le volume de dihydrogène H2 formé à la cathode connaissant l'intensité I du courant et la durée t de l'électrolyse.
Constante de Faraday / Volume molaire
/ Volume molaire / Tests de reconnaissance du dihydrogène et du dioxygène
/ Tests de reconnaissance du dihydrogène et du dioxygène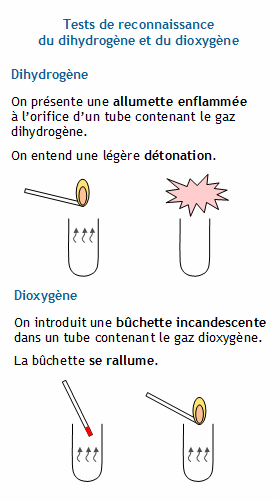
|
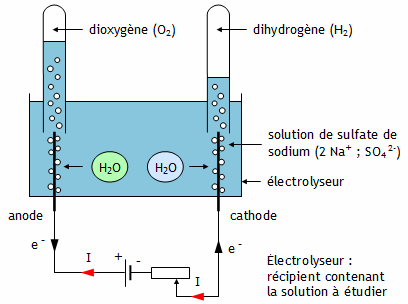
Taper les données Taper les nombres décimaux avec un point et non une virgule, Ne pas laisser d'espace vide entre les caractères. Électrolyse d'une solution de sulfate de sodium On utilise une solution de sulfate de sodium car elle contient des ions sodium Na+ et sulfates SO42- qui assurent la conduction du courant électrique dans la solution de l'électrolyseur. L'eau pure n'est pas conductrice contrairement à la solution aqueuse de sulfate de sodium. On a choisi comme électrolyte un sel (sulfate de sodium) mais on aurait pu choisir un acide (ex : acide sulfurique) ou une base (ex : soude). 1. Expérience On plonge deux électrodes métalliques dans une cuve remplie dune solution de sulfate de sodium. Ces électrodes sont ensuite reliées aux bornes dun générateur de tension continue.
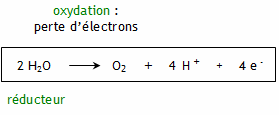
Le volume de dihydrogène est le double du volume de dioxygène. 2. Réactions aux électrodes Anode : Les électrons e- perdus par les molécules d'eau H2O sortent par lélectrode reliée à la borne positive du générateur. Cette électrode est donc le siège dune oxydation, c'est l'anode.
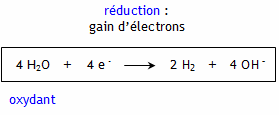
Cathode : Les électrons e- gagnés par les molécules d'eau H2O entrent par lélectrode reliée à la borne négative du générateur. Cette électrode est donc le siège dune réduction, c'est la cathode.
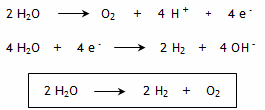
3. Bilan global : Il y a autant d'électrons captés à l'anode que d'électrons cédés à la cathode car il n'y a pas d'accumulation de charges électriques dans le circuit.
Le bilan global montre que la décomposition de l'eau forme deux fois plus de moles de dihydrogène que de dioxygène. Le volume de dihydrogène formé à la cathode est donc le double du volume de dioxygène formé à l'anode. |
 Des remarques, des suggestions ! |
© 2009 Editions Petite Elisabeth, tous droits réservés.
SIREN : 514 003 193
APE : 5811Z